抗米勒激素(AMH)(或米勒抑制物质,MIS)是转化生长因子-β(TGFβ)配体超家族的成员,对胎儿发育中的性别测定至关重要。在女性中,AMH及其II型受体(AMHR2)在卵巢卵泡(包括猫卵巢)的粒细胞中高度表达。近期的研究成果认为,由腺相关病毒(AAV)载体的基因治疗产生的AMH的超生理水平可以抑制成卵生成并诱导成年雌性小鼠的持久避孕。避孕机制与其他激素避孕药不同,主要作用于卵泡发育的早期与促性腺激素无关的步骤,抑制原始卵泡激活和前卵泡的成熟。
美国俄亥俄州动物园濒危野生动物保护和研究中心的研究者们使用载有猫抗米勒激素基因的腺相关病毒载体进行一次肌肉注射的方法,在家猫中实现长期避孕。在两项交配研究中测量交配行为和生殖成功。结果显示,抗米勒激素的异位表达不会影响性激素或发情周期,但阻止了繁殖引起的排卵,从而在雌性家猫中实现了安全且持久的避孕。研究成果以“Durable contraception in the female domestic cat using viral-vectored delivery of a feline anti-Müllerian hormone transgene”为题,发表在Nature Communications(IF:17.694)上。

猫AMH转基因的优化和AAV9载体的验证
实验验证:通过在裸鼠中进行腹腔注射,研究团队发现一个月后,AMH蛋白在多个组织中表达,包括四头肌和腹壁肌肉,以及肾脏、脾脏、胰腺和肝脏等腹腔器官。在接受AAV9-fcMISv2治疗的小鼠中,卵巢较对照组更小,并且卵巢中的初级、次级和囊泡的数量明显减少。这与先前使用人类AMH基因进行类似实验的结果相符。这些结果表明,通过AAV9载体成功传递了经过优化的猫AMH基因,在小鼠中引起了AMH的高效表达,并导致卵巢发生了变化。
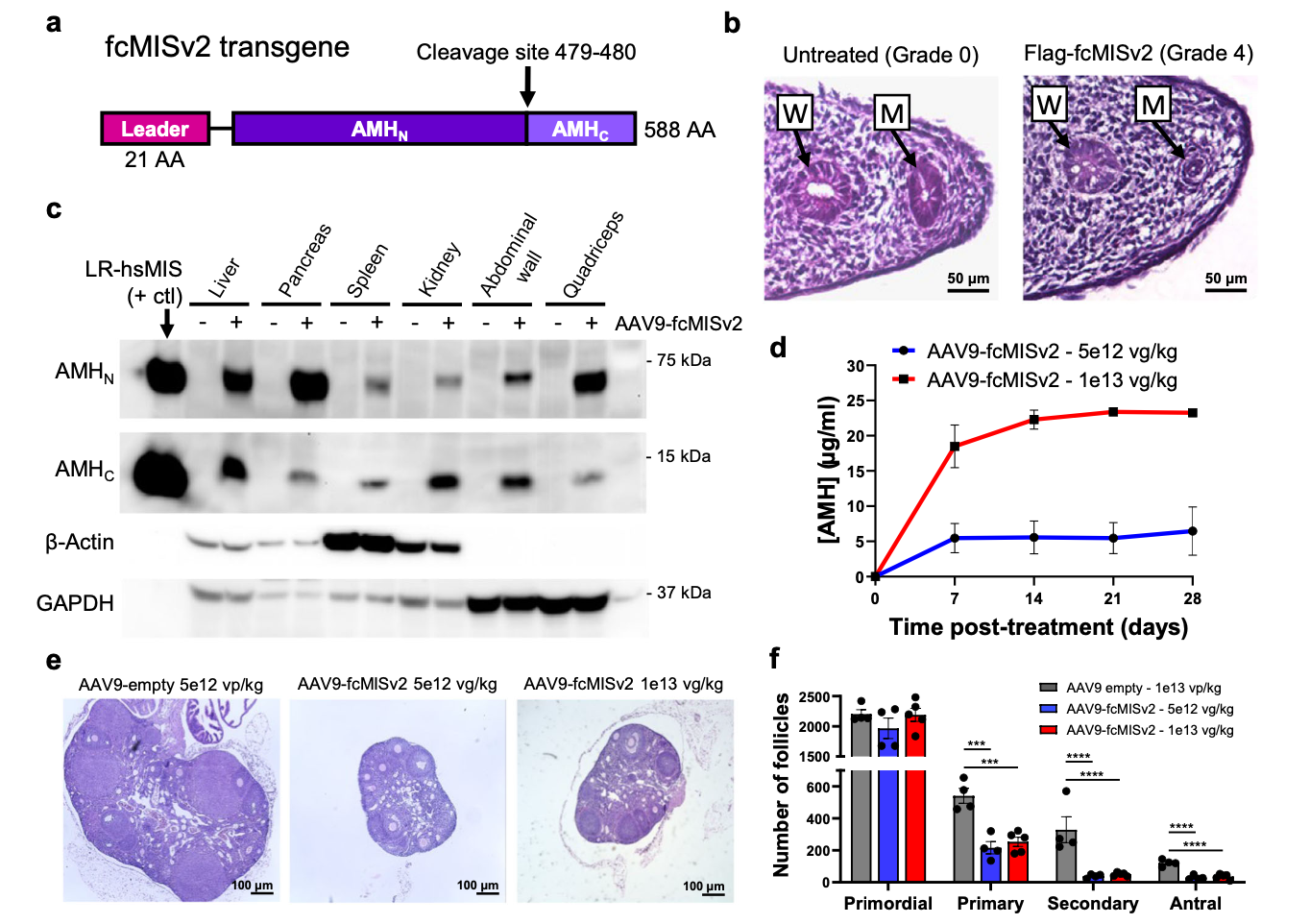
图1:小鼠中的fcMISv2。
a) 密码子优化猫AMH转基因(fcMISv2)的设计;
b) 胎儿大鼠泌尿生殖器脊段被未经处理的雌性的H&E染色(阴性对照);
c) 在用AAV9-fcMISv2(+)每公斤1e13病毒基因组(vg/kg)或AAV9-空载体控制(−)每公斤(vp/kg)5e12病毒颗粒治疗30天后,小鼠组织WB结果;
d) 用AAV9-fcMISv2的5e12 vg/kg(蓝色,圆圈)或1e13 vg/kg(红色,正方形)治疗小鼠中用ELISA测量的AMH血清浓度。n = 3个生物独立的动物。数据预发送为平均值± SEM;
e) 用AAV9-fcMISv2的5e12 vg/kg或AAV9-fcMISv2的5e12 vp/kg治疗四周后,小鼠卵巢的代表性中间部分,或AAV9-空载体对照的5e12 vp/kg;
f) 同一时间点整个卵巢的卵泡计数。
在猫中给予单剂量的第一代AAV9-fcMISv1载体会导致肌肉中延长AMH表达、可变抗转基因抗体反应和生殖道组织逻辑变化
作者对第一代AAV9-fcMISv1载体进行的实验。三只雌性家猫接受了该载体的治疗,剂量为每公斤体重5e12个病毒颗粒。观察到在治疗后没有明显的疼痛或注射部位的不适。血液检查显示轻微的炎症标志物上升,但迅速恢复。对AMH水平进行了4年的监测,同时也检测了对fcMISv1的抗体。在手术后,对其中三只猫的卵巢和子宫进行了组织学检查。其中一只猫表现出高AMH水平,抑制了卵巢功能,而其他两只由于抗体反应和AMH水平较低,导致子宫发生异常变化。最后,对一只猫进行解剖,发现AAV9-fcMISv1在骨骼肌中的表达较高,而在肝脏中表达较少。总的来说,这项研究表明AAV9-fcMISv1对猫的治疗效果在一些猫中可能更好,但在另一些猫中存在限制。
给予单剂量的AAV9-fcMISv2会导致持续分泌超生理AMH,没有不良反应或免疫反应
研究团队使用了第二代基因传递载体(AAV9-fcMISv2)来评估高水平AMH对猫生殖的影响。通过肌肉注射给予9只猫不同剂量的AAV9-fcMISv2或对照。实验结果显示,这一治疗方案在猫身上表现出较好的耐受性,未引起明显不适。血液检查和生理检查未显示出明显的异常,病毒基因组在体内的排泄持续了数月。与先前的基因传递载体相比,第二代载体未引起明显的抗体反应。血清中的AMH水平在第一年逐渐下降,但在第二年趋于稳定,保持在高水平。这些结果表明AAV9-fcMISv2可能是一种安全有效的方法,有望对猫的生育产生影响。
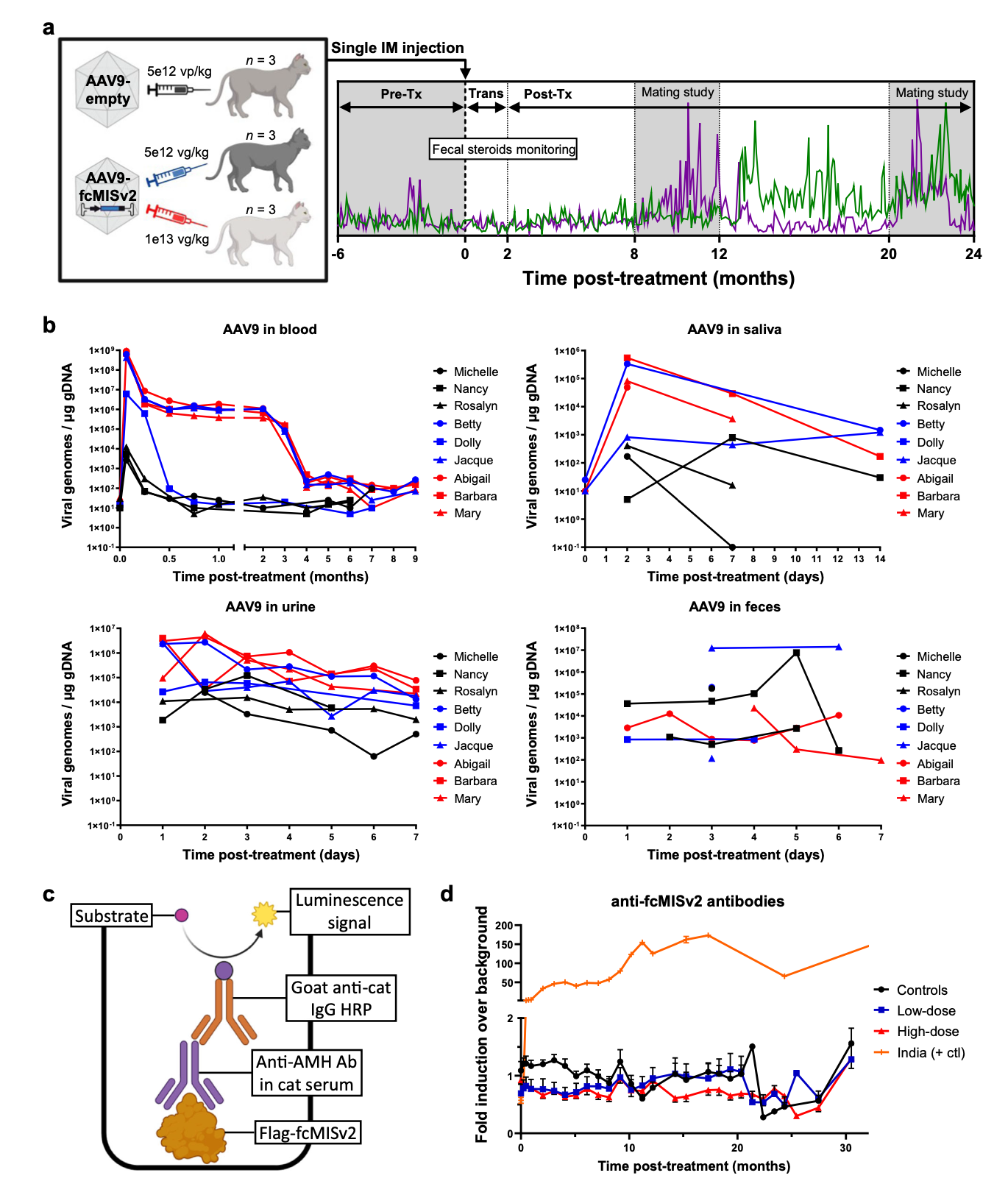
图2:家猫AAV9-fcMISv2注射的研究时间表和安全性。
a) 九只性成熟的雌性家猫接受了AAV9肌肉治疗;
b) 低剂量(蓝色)或高剂量(红色)AAV9-fcMISv2或AAV9-空载体控制(黑色)后,通过qPCR在家猫的血液、口腔拭子、尿液和粪便样本中进行病毒基因组量化;
c) 设计直接蛋白质捕获ELISA分析的图形表示,以测量猫血清中的抗fcMISv2 IgG;
d) 注射低(蓝色方块)或高剂量(红色三角形)AAV9-fcMISv2或AAV9-空矢量控制(黑圈)的雌性猫的平均血清抗fcMISv2抗体滴度(黑圈)。n = 3种生物独立动物。数据以平均值± SEM表示。“印度”(橙色加体征)的血清样本,一种对fcMISv1提高免疫反应的女性,被用作阳性对照。
超生理AMH诱导生殖激素和卵巢循环的变化
在治疗后的第8个月和第20个月启动了两个为期4个月的交配试验,使用不同的雄性猫进行每个试验。交配试验结果:对照组的雌性猫在试验中均怀孕并分娩,而接受AAV9-fcMISv2治疗的雌性猫未分娩。通过超声检查确认了对照组的妊娠,而治疗组未观察到孕囊或胎儿。统计数据表明,在两个交配试验中,接受治疗的雌性猫中,没有出现任何分娩,而对照组产下了健康的小猫。通过卡方检验发现,治疗组与对照组在允许交配的雌性数量、总交配次数、产生黄体期的次数、怀孕雌性数量以及总产仔数量等方面存在显著差异。
研究结果强烈暗示,超生理水平的AMH抑制了诱导排卵,导致在猫中产生避孕效果。实验中没有检测到治疗组雌性猫的产仔,进一步支持了AAV9-fcMISv2作为一种潜在的避孕方法。
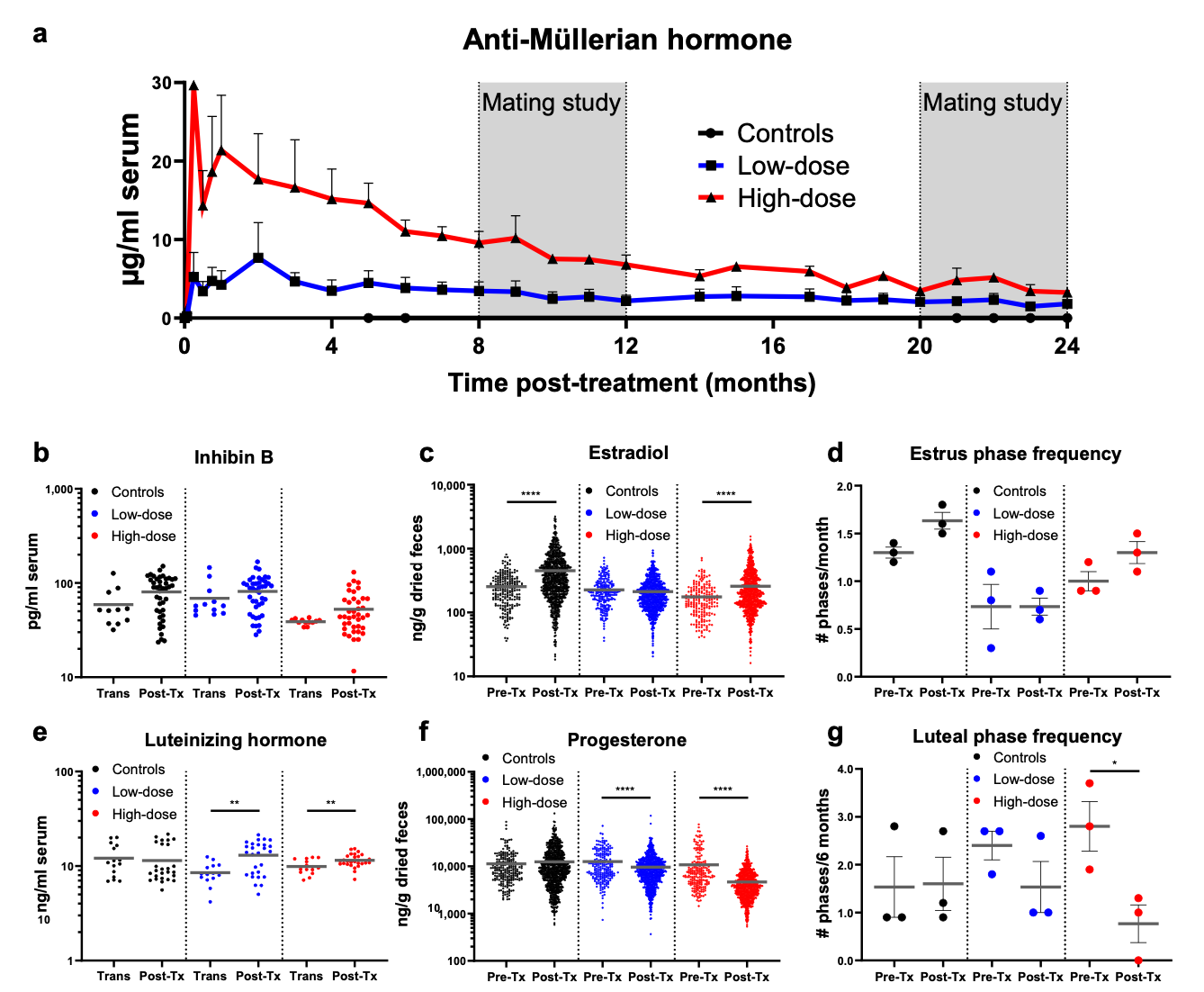
图3:家猫AAV9-fcMISv2注射后的生殖激素。
a) 在整个研究过程中,每月评估每公斤AAV9-fcMISv2每公斤(vg/kg)或AAV9-空载体(对照,黑色)接受5e12病毒基因组治疗的猫中AMH的平均血清浓度;
b) 低(蓝色)和高剂量(红色)组的抑制B水平,以及每公斤注射5e12 AAV9-空载体粒子(vp/kg)(对照组,黑色)的猫的抑制B水平;
c) 对每组猫在治疗前(Pre-Tx,注射前最多6个月)和治疗后期间收集的干燥粪便样本中雌二醇(E2)代谢物的浓度进行了比较;
d) 根据治疗前后的粪便类固醇剖面,评估发情期(≥2个连续样本,E2 > 1.5标准差于基线平均值)频率;
e) 血液中的黄体生成激素(LH)水平和f孕酮(P4)代谢物干粪便样本。g根据粪便类固醇剖面评估黄体期(≥6个连续样本,P4>1.5倍基线平均值)频率。B-g的水平线表示平均值。
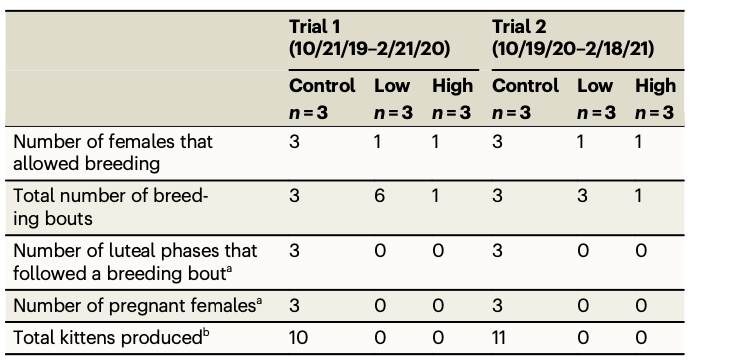
表1:在两次单独的交配试验中,AAV9-fcMISv2治疗的猫与对照组的育种活动、排卵和怀孕发生
总结:
这篇文章研究了一种在雌性家猫中实现持久避孕的方法。研究采用病毒载体传递猫抗-Müllerian激素基因,通过一次肌肉注射达到避孕效果。在实验中,对治疗后的雌性进行了两年多的跟踪观察,监测了抗基因表达、抗抗基因抗体和生殖激素水平。结果显示,这种方法不影响性激素或发情周期,但能够阻止繁殖引起的排卵,从而在雌性家猫中实现了安全而持久的避孕效果。这一研究为发展更为高效、无创和成本效益的宠物避孕方法提供了有益的证据。
