01
常用的 3D 生物打印技术
三维 (3D) 生物打印 (Three dimensional (3D) Bioprinting) 是利用活细胞、生物分子和生物材料 (生物墨水, 如水凝胶) 打印生物医学结构的方法,通过逐层沉积生物材料以创建组织和器官等 3D 结构[1][2]。
例如,传统的组织工程策略首先需要将细胞接种到多孔水凝胶支架上。随后在体内培养,这些细胞发生增殖和分化,最终构建生物替代品。

图 1. 用于组织工程的 3D 生物打印结构[3]。
知识链接:
3D 生物打印是 3D 打印的一种延伸,它以增材制造技术为基础,可在 X、Y 和 Z 方向控制制造 3D 结构。要形成的复杂结构可以使用计算机辅助设计 (CAD) 软件进行设计,也可以从磁共振成像 (MRI) 或计算机断层扫描 (CT) 等医学图像中进行扫描[4]。
目前,3D 生物打印已成为一种很有前途的技术,可用于制造具有定制生物成分和机械性能的复杂组织结构。
应用:
(1) 通过利用这种变革性技术,可以精确定位生物墨水(包括水凝胶、细胞和生长因子),以创建 3D 体外培养环境;
(2) 也可以在体外重现天然组织结构、细胞组成和脉管系统,以创建仿生组织模型;
(3) 还可用于研究疾病机制、筛选药物和其他临床应用[4]。
(4) 此外,随着诱导性多能干细胞(iPSC)衍生细胞的进一步参与,可以建立健康和疾病状态下的个性化组织模型,以定制药物筛选和治疗过程。

图 2. 使用 3D 生物打印构建可用于药物测试和疾病建模的体外结构[4]。
目前,常见的 3D 生物支架打印技术主要包括喷墨打印(Inkjet-based)、挤出打印(Extrusion-based) 和光辅助打印 (Light-assisted) 等。
每种打印方法都能打印细胞支架和直接在支架内封装细胞以构建组织构造[4]。这些平台在打印机制、分辨率、时间和材料选择等方面存在差异。挤出打印是最常用的技术,其次是光辅助和喷墨打印[5][6][7]。下表总结了目前常用的几种 3D 生物支架打印技术的区别。
表 1. 不同 3D 生物打印之间的区别[2][4-12]。


02
生物墨水
3D 生物打印借由 3D 生物打印机,制造出细胞支架,再将细胞"种入"支架中,使细胞得以生长[13]。
支架作为细胞相互作用的模板,为新发育的组织提供物理支持[14]。此外,支架还可以作为运载工具,加入必需的生长因子来控制和促进组织生长[15]。因此,支架打印在 3D 打印中十分重要,是 3D 打印的起始阶段。
用于生物打印支架的材料被称为生物墨水,生物墨水由生物材料溶液和细胞 (存在或不存在生长因子) 组成,包括单一类型的生物材料或各种生物材料的混合物[6]。
表 2. 不同生物墨水之间的区别[16][17]。
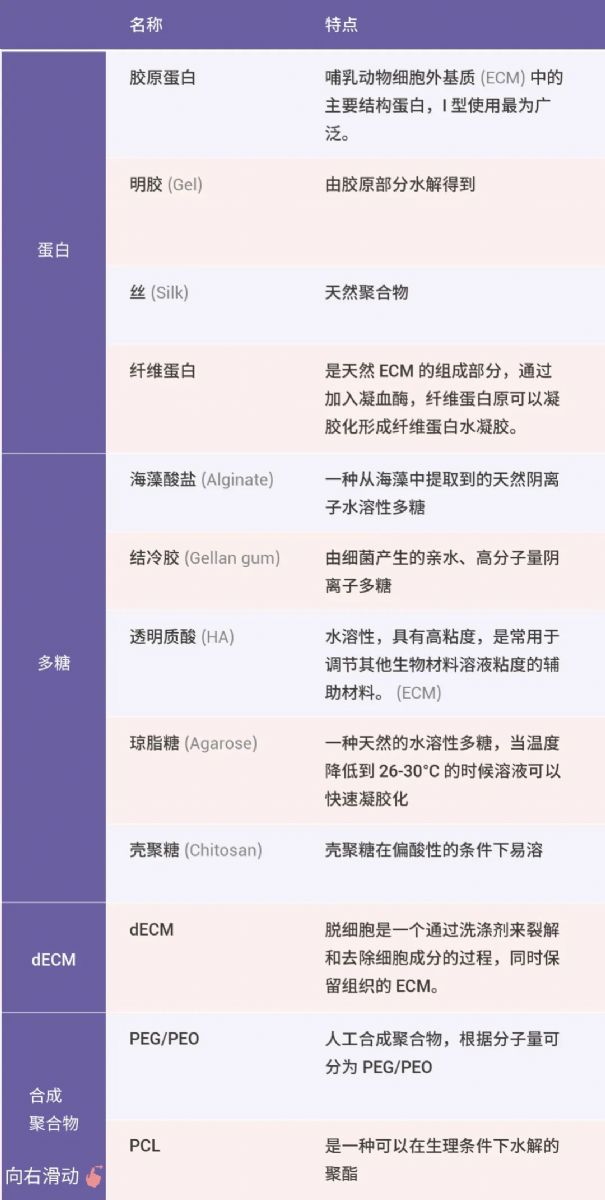
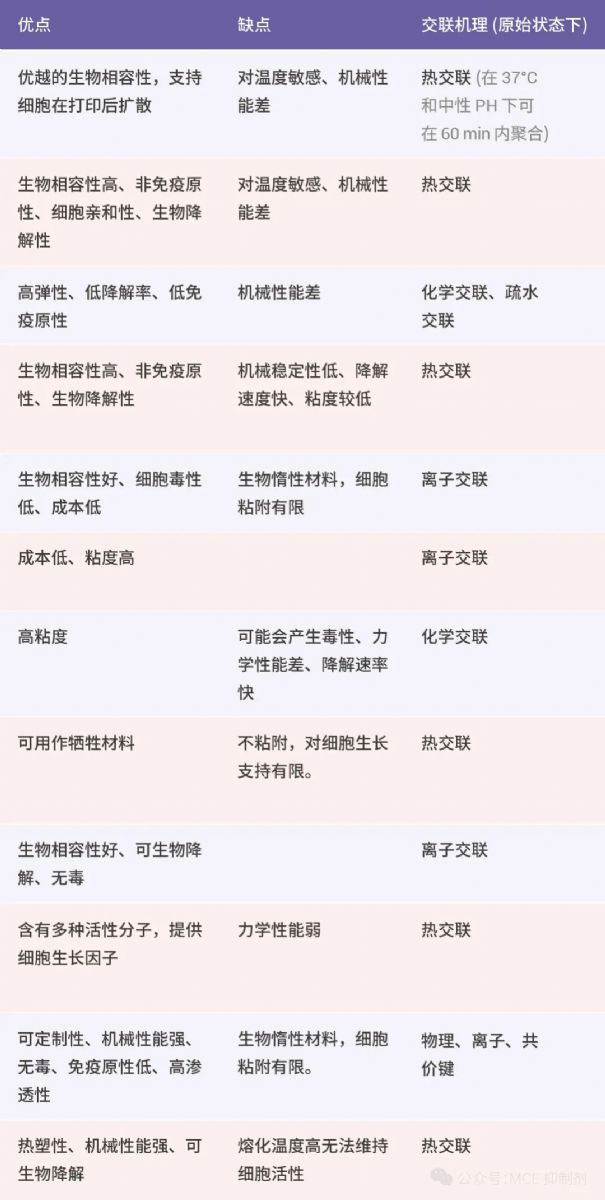
生物墨水可以根据其来源分为天然聚合物和合成聚合物两大类。
- 天然聚合物 (如藻酸盐、壳聚糖、明胶、胶原蛋白) 有着与人体 ECM 的相似性及其固有的生物活性,但可能在机械性能上存在限制。
- 合成聚合物 (如聚己内酯 PCL、聚乳酸 PLA、聚乙二醇 PEG),虽然通常在生物学上是惰性的,但它们机械性能较强且具有可控的物理化学性质 (降解率、扩散率、疏水性)[16]。
生物墨水的选择取决于特定的应用 (例如不同的组织、不同的打印方法),在 3D 打印过程中选择生物墨水主要依据以下几点:
- 一定的机械性能 —————— 能提供支架支撑
- 精确沉积、快速凝固 ———— 提高打印分辨率
- 可降解、无毒 ——————— 减少细胞损伤
- 墨水流动性 ———————— 保持打印结构
- 生物相容性 ———————— 支持细胞生长/发挥正常功能
- 免疫原性 ————————— 植入体内后不引起免疫反应
03
生物墨水的交联原理
打印形成支架后,3D 生物打印中使用的生物墨水要通过交联形成水凝胶,以达到保持打印结构保真度和分辨率所需的强度和稳定性。此外,水凝胶的交联可以为打印结构内的细胞生长提供足够的支持。水凝胶的交联途径包括化学交联和物理交联[3]。
- 物理交联是发生在各种聚合物链之间的非共价键相互作用,如疏水、静电、氢键、立体络合和主客相互作用,物理交联的过程一般在温和的生理条件下实现,但这种交联是可逆的[18]。
- 化学交联的反应通过交联剂或者通过自然形成的共价键实现,这些键的形成可以通过自由基聚合、酶促或互补基团的反应来诱导[19]。化学交联不可逆,但交联剂的选择很重要,否则可能会对细胞造成一定的损伤[20]。
表 3. 物理交联和化学交联原理。

在生物墨水的交联使用中,物理交联这类非共价键的交联往往不太稳定,不完全交联可能导致结构坍塌从而失去形状,因此选择正确的交联方式对维持模型的稳定十分重要。
光交联反应是目前使用较为广泛的交联方式,这是因为光交联不仅交联速度快而且产热较小[21]。同时光基生物打印可以通过光敏材料的光聚合来实现,生物墨水只需要与光反应基团相结合就可以实现快速光聚合 (如图 1)[22]。目前市面上常用的光反应基团是甲基丙烯酰基 (Mal)。

图 3. 光交联原理[3]。
通常,紫外光和可见光均可用作光聚合的光源 (Light source)。然而,由于紫外光可能诱发基因突变,甚至导致细胞死亡,因此在基于光的生物打印中通常使用可见光源来确保细胞活力并避免对细胞造成潜在伤害。光引发剂 (Photo-initiators,PIs) 是感光生物墨水的关键成分。当受到光照射时,PI 可以被激发产生活性物质,随后引发生物材料的聚合。04
小结
在这篇文章里,我们介绍了 3D 生物打印的原理、当前常用的生物打印技术、生物墨水的交联原理及选择。3D 打印的成功与否是与这些因素息息相关的,除此之外打印时间、速度、压力以及细胞材料的选择同样也很重要。
| 产品推荐 |
| Green Fluorescent Gelatin Methacryloyl (HY-158217) 带有绿色荧光的甲基丙烯酰化明胶 |
| Red Fluorescent Gelatin Methacryloyl (HY-158218) 带有红色荧光的甲基丙烯酰化明胶 |
| Blue Fluorescent Gelatin Methacryloyl (HY-158219) 带有蓝色荧光的甲基丙烯酰化明胶 |
| Chondroitin Sulfate Methacryloyl (HY-158221) 甲基丙烯酰基化的硫酸软骨素 |
| Alginate Methacryloyl (HY-158222) 甲基丙烯酰基化的海藻酸盐 |
| Carboxymethyl chitosan Methacryloyl (HY-158223) 甲基丙烯酰基化的羧甲基壳聚糖 |
| Silk Fibroin Methacryloyl (HY-158224) 甲基丙烯酰基化的丝素蛋白 |
参考文献:
[1] Derakhshanfar S, et al. 3D bioprinting for biomedical devices and tissue engineering: A review of recent trends and advances. Bioact Mater. 2018 Feb 20;3(2):144-156.
[2] Cui X, et al. Thermal inkjet printing in tissue engineering and regenerative medicine. Recent Pat Drug Deliv Formul. 2012 Aug;6(2):149-55.
[3] Zhang X, et al. Applications of Light-Based 3D Bioprinting and Photoactive Biomaterials for Tissue Engineering. Materials (Basel). 2023 Nov 30;16(23):7461.
[4] Ma X, et al.3D bioprinting of functional tissue models for personalized drug screening and in vitro disease modeling. Adv Drug Deliv Rev. 2018 Jul;132:235-251.
[5] Gao Q, et al. Coaxial nozzle-assisted 3D bioprinting with built-in microchannels for nutrients delivery. Biomaterials. 2015 Aug;61:203-15.
[6] Zhang J, et al.3D Bioprinting of Human Tissues: Biofabrication, Bioinks, and Bioreactors. Int J Mol Sci. 2021 Apr 12;22(8):3971.
[7] Fang W, et al. Light-based 3D bioprinting technology applied to repair and regeneration of different tissues: A rational proposal for biomedical applications. Mater Today Bio. 2024 Jun 26;27:101135.
[8] Wang J, et al. Stereolithographic (SLA) 3D printing of oral modified-release dosage forms. Int J Pharm. 2016 Apr 30;503(1-2):207-12.
[9] Jacobs, Paul F, et al.Stereolithography and Other Rp&m Technologies: From Rapid Prototyping to Rapid Tooling. 1995 Oct 1.
[10] Wang Z, et al.3D bioprinting in cardiac tissue engineering. Theranostics. 2021 Jul 6;11(16):7948-7969.
[11] Wu, Lifang & Zhao, et al. EHMP-DLP: multi-projector DLP with energy homogenization for large-size 3D printing. Rapid Prototyping Journal. 2018 Nov 24:1500-1510.
[12] Chang, et al. The Influence Analysis of Globular Indexing Cam Mechanism Size Parameters on Transmission Performance. Advanced Materials Research.2012 Jan 426:163-167.
[13] Sears NA, et al. A Review of Three-Dimensional Printing in Tissue Engineering. Tissue Eng Part B Rev. 2016 Aug;22(4):298-310.
[14] Wu Z, et al. Bioprinting three-dimensional cell-laden tissue constructs with controllable degradation. Sci Rep. 2016 Apr 19;6:24474.
[15] Liu X, et al. Delivery of growth factors using a smart porous nanocomposite scaffold to repair a mandibular bone defect. Biomacromolecules. 2014 Mar 10;15(3):1019-30. doi: 10.1021/bm401911p. Epub 2014 Feb 3. PMID: 24467335.
[16] Chen XB, et al.Biomaterials / bioinks and extrusion bioprinting. Bioact Mater. 2023 Jun 27;28:511-536.
[17] Gungor-Ozkerim PS , et al.Bioinks for 3D bioprinting: an overview. Biomater Sci. 2018 May 1;6(5):915-946.
[18] Hennink WE, et al. Novel crosslinking methods to design hydrogels. Adv Drug Deliv Rev. 2002 Jan 17;54(1):13-36.
[19] Hu W , et al. Advances in crosslinking strategies of biomedical hydrogels. Biomater Sci. 2019 Feb 26;7(3):843-855.
[20] GhavamiNejad A, et al. Crosslinking Strategies for 3D Bioprinting of Polymeric Hydrogels. Small. 2020 Sep;16(35):e2002931.
[21] Lim KS, et al. Fundamentals and Applications of Photo-Cross-Linking in Bioprinting. Chem Rev. 2020 Oct 14;120(19):10662-10694.
[22] Bagheri A , et al.Photopolymerization in 3D Printing.ACS Applied Polymer Materials, 2019, 1(4).DOI:10.1021/acsapm.8b00165.
