
干粉发生器,粉尘发生器,干粉药物雾化器
产品名称: 干粉发生器,粉尘发生器,干粉药物雾化器
英文名称: 干粉气溶胶发生器,粉尘气溶胶发生器
产品编号: 干粉发生器,粉尘发生器
产品价格: 0
产品产地: USA
品牌商标: 玉研仪器公司
更新时间: 2023-08-17T15:24:17
使用范围: null
- 联系人 : 方经理
- 地址 : 上海市闵行区兴梅路485号中环科技园301室
- 邮编 : 200237
- 所在区域 : 上海
- 电话 : 185****9044 点击查看
- 传真 : 点击查看
- 邮箱 : sales@yuyanbio.com
干粉发生器可以将粉末状的样品雾化出细小的粉尘气溶胶颗粒,在扩散器中气流将被加速到 180m/s 的高速度,处在扩散头部位的样品在高速度气流带来的湍流和剪切力的作用下,团聚的颗粒被分散开来,呈气溶胶状态随气流被均匀吹出,形成实验所需要的粉尘气溶胶。
根据实验需求,可以将特定药物或者污染物的粉尘气溶胶引入到全身暴露舱或者口鼻暴露塔中,对动物进行暴露染毒实验;也可将特定的粉尘气溶胶引入到密封的容器中,形成一定浓度的粉尘和扬尘环境,用于空气净化 方面的研究。
主要特点:
· 可对非常微量的粉末进行扩散;
· 可以对贵重、有毒性的样品进行扩散;
· 可用来将粉尘引入颗粒度仪,散射出干的聚苯乙烯胶乳球体(PSLs)来标定测量仪器;
· 可用于环境监测滤膜上收集到的颗粒物进行再分散等;

型号:YAN-S200
技术参数:
· 粒径范围:0.1~10μm
· 微调模式质量流量范围:200mg/h-20g/h
· 微调模式下体积流量范围 0-5L/min(0-0.3m3/h)
· 可通过空气泵和流量控制器,对粉尘气溶胶进行稀释,流量为:0-20L/min
· 全开模式质量流量范围:20-100g/h
· 流量控制范围:0/5L/min,0-10L/min,0-30L/min可选
· 采用4.3寸触摸屏,控制方便
· 两种药仓可选,直径分别为:8mm,20mm
· 速度可调:1-20r/min
· 带间歇控制模式,时间控制精度为1s,可调范围:1-99s
· 电源要求:220V/50Hz
· 主机尺寸:26*18*32cm 长*宽*高
· 重量:6kg
根据需要,还可以选择:410型粉尘发生器:

型号:410型
410是一种通用的干粉气溶胶扩散器,其在气溶胶及粉体研究方面有广泛应用。
使用传动牙轮皮带将粉末定量输送至扩散器,经过精心设计的齿间距即使是在低供料率的情况下可以持续稳定地输送粉末。通过调节送料皮带的速度,可轻易地大范围调节输出气溶胶的浓度。当粉末从喷嘴中输出时,在喷嘴口形成的剪切力将团聚的粉末微粒分散开,从而形成气溶胶颗粒。专用的刮料装置可保证带齿间的填料均衡,从而将储槽中的粉末多少对气溶胶质量流量的影响减到尽量小。
仪器操作及特点:
- 可在较宽范围内持续稳定地供料
- 换料和清洁均十分方便
- 精度高、基本不受储槽中粉尘多少的影响
- 设备运行中的再填料不会影响到气溶胶质量浓度--持续长时间研究的理想选择。
- 即使是低流量时仍可达到高浓度--可加快低流量情况下的应用研究。
- 扩散头可更换,故一台设备的输出范围可在1~6000 g/h 内连续可调
- 使用手动和微机远程控制的单元均可
仪器标定:SAG的质量输出量可进行定义。用户可以通过调节送料带的速度来调整输出所需的容积流量。下表为容积流量和送料带速度的关系图。固体物质的质量流量取决于其体积密度,而体积密度可通过测量一定时间内输送的物质质量轻易算出。下表画出了几个输出标度的示例。一旦输出标度确定后,用户便可轻易地调节所需的物质质量输出量。
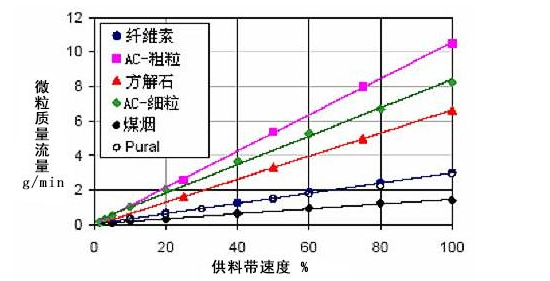
仪器规格参数:
- 颗粒类型:非粘性干粉
- 连续运行时间:1~50 h
- 压缩空气要求:zui大6bar
- 储粉罐容积:320cm3(410/L)、320cm3(410) 、1420cm3(410/H)
- 粉尘喂料流量:5~278cm3/h (410/L)、10~557cm3/h (410)、120~6487cm3/h (410/H)
- 粉尘质量流量:1~264g/h (410/L)、9.5~529g/h (410)、114~6162g/h (410/H)
- 气溶胶体积流量:0.5~2.5m3/h (410/L)、0.5~2.5m3/h (410)、5~20m3/h (410/H)
- 气溶胶出口浓度:1~264mg/m3 (410/L)、1.9~529mg/m3 (410/L)、5.7~1232mg/m3 (410/L)
- 电源要求:100~260VAC/47~63Hz
- 仪器尺寸:D 320 x W 400 x H 320mm
- 仪器重量:12 kg
根据实验需求,您可能需要气溶胶发生器、动物暴露染毒箱:
气溶胶雾化器能够产生稳定、细腻的气溶胶,给动物暴露实验或者细胞暴露实验提供稳定的雾化环境。
气溶胶雾化器是全身暴露或者口鼻暴露的重要组成部分,可配合暴露箱或者暴露塔使用,将药物雾化后的气溶胶推送到暴露内,并持续雾化和维持暴露箱内一定的气溶胶浓度。
我们可以提供Aerogen Pro雾化器和Aerogen Solo雾化器:设备采用钯合金振动网格技术,中心孔板直径5mm,均匀分布着1000个精密成形微孔,每秒振动128,000次,形成非常有利于沉淀入肺部沉积的气溶胶颗粒滴。
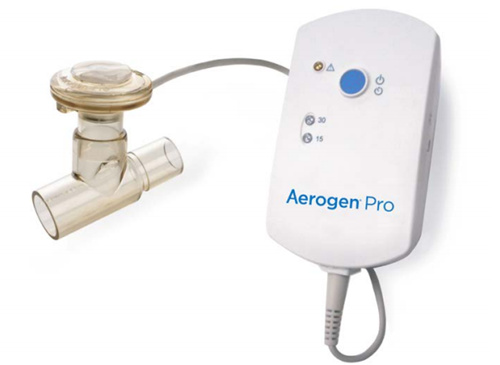
型号:Aerogen Pro

型号:Aerogen Solo
产品主要优势:
无论短时程和长时程实验都能保证出色地输出持续一致;
雾化剂量小;
粒度分布和颗粒物体浓度具有高度的可重复性;
随时可填充药物,也可以加配注射泵自动添加药物;
抗腐蚀外壳设计,持久耐用;
高度集成化、体积小巧;
操作简单,无需复杂的培训工作;
雾化头的主要参数:
小型:Volume Median Diameter(VMD)
雾化速率: >0.1mL/min
颗粒尺寸: VMD (体积中值直径)介于2.5μm and 4.0μm
药物残余量: <0.1mL
雾化器连接示意图:
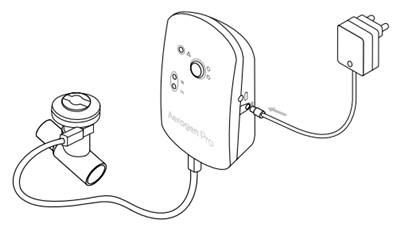
雾化的颗粒物粒径分布:
根据需要,您还可以选择BGI Collison气溶胶发生器

MRE型Collison气溶胶发生器是由英国波顿的Microbiological Research Establishment设计的平底型喷雾器,有1喷嘴,3喷嘴和6喷嘴多种型号可选,3喷嘴是最常用的型号。
金属部件都是由316不锈钢加工而来,O型圈是橡胶或硅橡胶,玻璃罐是冕牌玻璃制成。
BGI喷雾器顶部的”T”形杆既提供了空气进口,又可以连接了压力表。
24 Jet Collison型号的喷雾器(24喷嘴的型号)是6喷嘴MRE改良型的扩大版。它有一个32盎司,干净覆膜的瓶子,以保持和3喷嘴、6喷射喷雾器相同的墙板间距尺寸,能够输出4倍左右于6喷嘴相同特性的气溶胶,但最大压力需要限制在30 PSIG。
下图是Collison气溶胶发生器配套动物染毒箱、压缩泵进行动物整体暴露染毒的图片:

气溶胶雾化暴露箱(大鼠、小鼠气溶胶染毒箱,全身暴露系统)可将药物、致敏原或其他混合物雾化为极细微的气溶悬浮颗粒送入置放动物的箱体中,动物按实验预定的时间曝露于其中,完成动物建模所需的致敏和激发过程;也可作为全身暴露系统对动物进行全身暴露;
(玉研仪器公司,可以根据客户需求订做特殊气体的染毒箱,如:二氧化碳控制箱、二氧化#硫染毒箱、一氧化碳染毒箱、氧气浓度控制箱等,欢迎来电咨询)
有多种尺寸和规格的暴露箱可供选择,还可根据需求进行订做:
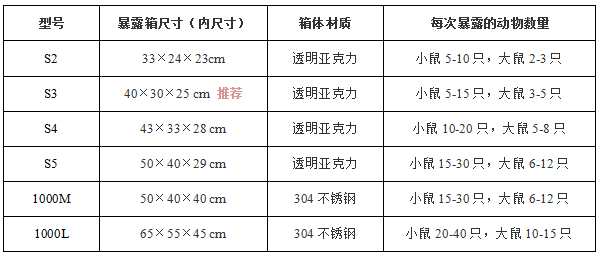
注:实际容纳数量与动物的周龄和体重的不同而有所不同。根据药物特性,雾化和暴露装置最好在生物安全柜中使用。

全身暴露系统的主要特点:
· 同时针对多只动物建模,节省时间,一致性好。
· 根据有关文献,以OVA致敏为例,雾化方式建模比腹部注射方式所需时间短。
· 一体化的控制仪同时具有定时器功能、雾化参数设定及0~5LPM偏流供风系统。
· 偏流供风可在较长时间的致敏过程中为箱体内的动物提供新鲜空气,并保持箱体内的温度湿度不会过高。
· 提供雾化颗粒直径2.5~4μm和4~6μm两种雾化头供选择。
根据实验需要,还可以选择口鼻暴露式染毒方法:
Ø 暴露迅速,浓度均匀,短时间内即可达到暴露浓度
Ø 只通过动物的鼻部呼吸接触到被测物质,有效防止动物的皮肤、口腔接触到被测物质
Ø 通过检测动物的胸扩运动,实时监测动物的呼吸频率和吸入量
Ø 采用双层塔结构设计,保证试样吸入浓度均匀;
Ø 同时,容易调控试样浓度,对浓度变化反映迅速且死体积小,能够在短时间内达到浓度平衡。
Ø 可根据需要选择合适的配置,一次对多可同时暴露6-24个实验动物
口鼻暴露塔主要构造及抛面图:
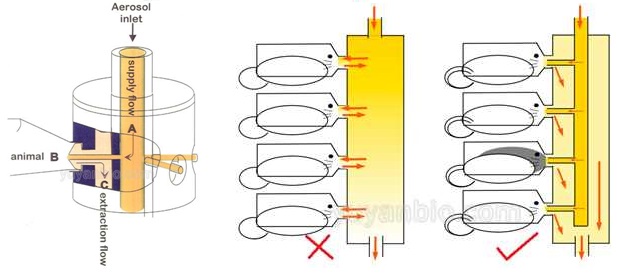
结构紧凑,对浓度变化反映迅速,并且死体积小,能够在短时间内达到浓度均衡;
采用双层塔结构设计,每只动物的呼吸经由不同的呼吸路径,每只动物接触到的气溶胶浓度都一致;
暴露塔内气溶胶单向流动,确保每只动物接触的气溶胶没有被其他动物影响;
不同型号的口部暴露塔:单层、双层、四层

根据动物数量选择合适的型号:每层6个通道,三种型号可分别对6只,12只,24只鼠进行暴露实验。
适合不同体重的大鼠和小鼠固定器:

动物呼吸参数测量系统
根据需要可以选配呼吸参数测量系统,用于对动物的各种呼吸参数进行检测和统计;
测量参数:气溶胶累积量,呼吸频率,呼气峰值,吸气峰值,呼气时间,吸气时间,呼气最大流量,吸气最大流量,潮汐量,呼气末暂停,吸气末 暂停、分钟呼吸量等
组配呼吸参数测量系统后的构造图:
呼吸参数测量软件界面:
1.Sidler-Moix A L, Di Paolo E R, Dolci U, et al. Physicochemical aspects and efficiency of albuterol nebulization: comparison of three aerosol types in an in vitro pediatric model[J]. Respiratory care, 2015, 60(1): 38-46.
2.Hassan A, Rabea H, Hussein R R S, et al. In-vitro characterization of the aerosolized dose during non-invasive automatic continuous positive airway pressure ventilation[J]. Pulmonary Therapy, 2016, 2: 115-126.
3.ElHansy M H E, Boules M E, El Essawy A F M, et al. Inhaled salbutamol dose delivered by jet nebulizer, vibrating mesh nebulizer and metered dose inhaler with spacer during invasive mechanical ventilation[J]. Pulmonary pharmacology & therapeutics, 2017, 45: 159-163.
4.Fang T P, Lin H L, Wan G H, et al. In vitro evaluation of aerosolized delivery of various medications during mechanical ventilation[J]. 2017.
5.Abdelrahim M E A, Saeed H, Harb H S, et al. The Aerosol Generators Available for Critically Ill Patient[J]. Essentials of Aerosol Therapy in Critically ill Patients, 2021: 115-135.
6.ElHansy M H E, Boules M E, El Essawy A F M, et al. Inhaled salbutamol dose delivered by jet nebulizer, vibrating mesh nebulizer and metered dose inhaler with spacer during invasive mechanical ventilation[J]. Pulmonary pharmacology & therapeutics, 2017, 45: 159-163.
7.Gowda A A, Cuccia A D, Smaldone G C. Reliability of vibrating mesh technology[J]. Respiratory Care, 2017, 62(1): 65-69.
8.Gerde P, Nowenwik M, Sjöberg C O, et al. Adapting the aerogen mesh nebulizer for dried aerosol exposures using the preciseinhale platform[J]. Journal of aerosol medicine and pulmonary drug delivery, 2020, 33(2): 116-126.
9.Michotte J B, Staderini E, Le Pennec D, et al. In vitro comparison of a vibrating mesh nebulizer operating in inspiratory synchronized and continuous nebulization modes during noninvasive ventilation[J]. Journal of aerosol medicine and pulmonary drug delivery, 2016, 29(4): 328-336.
10.Cahill R A, Dalli J, Khan M, et al. Solving the problems of gas leakage at laparoscopy[J]. British Journal of Surgery, 2020, 107(11): 1401-1405.
11.Sarhan R M, Elberry A A, Abdelwahab N S, et al. Effect of a nebulizer holding chamber on aerosol delivery[J]. Respiratory care, 2018, 63(9): 1125-1131.
