信使核糖核酸(Messenger RNA,mRNA)技术开辟了疫苗学的新纪元。这篇综述简要介绍了mRNA疫苗的发展,以及mRNA与纳米递送系统产生的先天免疫反应。
The rise of mRNA vaccines
mRNA疫苗领域在新冠疫情中得到了快速发展,辉瑞/BioNTech 和Moderna分别研制的两款mRNA新冠疫苗更首先获得美国FDA的紧急使用授权1,使得mRNA疫苗受到大众的广泛关注。事实上,mRNA技术建立在多年的研究基础之上,其概念验证研究最早可以追溯到三十多年前,当时Wolff et al.注意到将裸mRNA注射到小鼠骨骼肌能够在小鼠体内实现外源性蛋白的表达2。之后在1990年代的研究mRNA也被证明可以在体外和体内引发体液和细胞免疫反应3。不过,碍于mRNA本身结构不稳定,在体内应用后很容易降解,以及会诱发不必要的先天免疫反应3,mRNA技术有很长一段时间被认为其临床应用性较低。随着近十多年科学的进步,这些mRNA疫苗的研发难点逐渐被克服,例如通过进行化学修饰使mRNA增加稳定性和调节免疫原性、使用纳米粒子技术提高mRNA的胞内表达和递送效率等。其中,脂质纳米颗粒(LNP)是当前最主流的mRNA疫苗的纳米递送系统。LNP-mRNA技术平台现时已被广泛应用在各种疾病(如癌症、传染病或遗传疾病)的预防性疫苗或治疗性疫苗的临床前或临床研究4。
Overcoming the innate immune responses
mRNA是由DNA作为模版转录而來、带有蛋白质合成编码信息的一类单链RNA(ssRNA)。合成mRNA可以通过体外转录酶促反应(in vitro transcription enzymatic reaction,IVT)产生3。不过,由于RNA具有天然的免疫刺激特性,在进入细胞时,外源的体外转录mRNA会被机体免疫防御系统的第一道防线识别,激活不同的模式识别受体(PRRs),例如位于内体的TLR7/85。而IVT制备过程除了产生目的产物mRNA本身外,还会产生各种副产物。其中主要的副产物双链RNA(dsRNA)可以被TLR3和细胞质中的RIG-I/MDA-5特异性识别5。PRRs对RNA的感知会触发信号转导级联反应,导致产生IFN-α和IFN-β等I型干扰素和促炎性细胞因子(见图1)5。这些先天免疫激活可以有不良的影响,它们可以抑制mRNA的翻译和蛋白抗原合成,甚至引发细胞死亡,最终降低mRNA疫苗的有效性。
为了克服这种先天免疫应答,Karikó et al.首先尝试化学修饰IVT mRNA,他们通过使用天然存在的假尿苷(Pseudouridine,Ψ)来替换RNA序列的尿苷碱基6。这种修饰模拟内源性mRNA,成功减少了mRNA与机体的TLR7/8和其他免疫传感器的结合,限制I型IFN的过度产生并提高mRNA的翻译能力6。除了Ψ,常用的mRNA修饰还有N1-甲基伪尿苷(N1-methylpseudouridine,m1ψ)。研究发现与ψ修饰相比,引入m1ψ的mRNA序列在增强蛋白表达的能力和逃脱机体天然免疫应答的表现更好,尤其是在减少TLR3激活反应方面7。此外,为了进一步避免不必要的先天免疫激活,从IVT mRNA中去除dsRNA杂质是非常重要。IVT mRNA的纯化方法可以通过基于微珠的沉淀和色谱方法来实现,例如高效液相色谱(HPLC)4。
Formulating mRNA with LNPs
经修饰的mRNA转录物可以依靠LNP载体来保护其免于被细胞外的RNA酶(RNAse)降解,协助其顺利进入细胞和内体逃逸3。不过,载体分子也可以与疫苗的免疫原性相关。LNP通常由不同比例的磷脂、胆固醇、可电离/阳离子脂质和PEG-脂质组成4。尽管磷脂和胆固醇作为天然的细胞膜成分不太可能触发显著的先天免疫应答,但一些可电离/阳离子脂质可以通过激活PRR通路诱导炎症反应8。例如,Lonez et al.发现diC14-amidine脂质体可刺激TLR49;另一种阳离子脂质RPR206252也被发现可以通过TLR2和NLRP3通路激活炎症反应10。此外,其他成分如PEG被指出可以激活补体系统,触发机体的超敏反应。LNP递送系统的设计依然需要持续优化,充分评估不同组件成分的炎症性质,以调节与体内的先天免疫系统的相互作用。
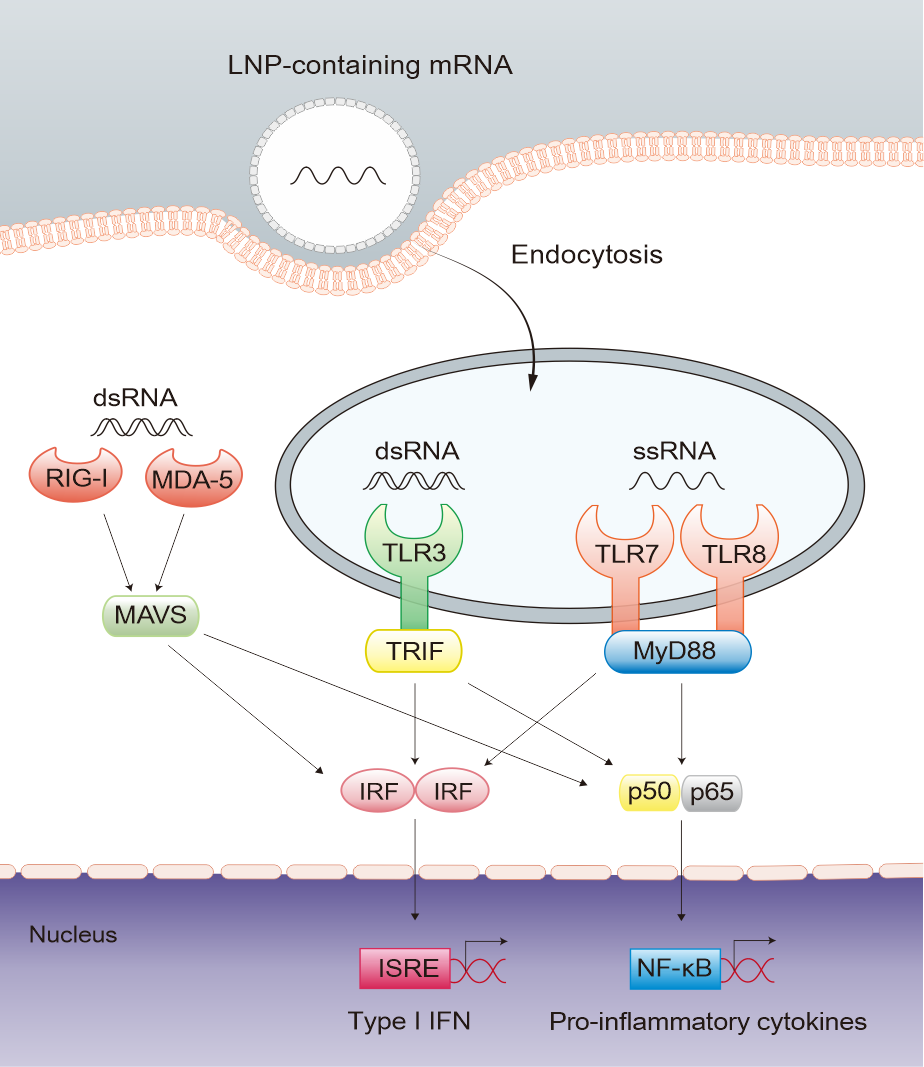
Fig. 1: IVT mRNA and dsRNA byproducts-induced immune activation
Innate immune activation assessment
先天免疫感应机制对mRNA疫苗可能是一把“双刃剑”。如上文所述,它可能抑制蛋白表达或导致过度的炎症反应;不过,预防性疫苗或某些类型的癌症疫苗可能会受益于其佐剂效应12。例如有研究显示辉瑞/BioNTech的新冠mRNA疫苗BNT162b2在小鼠体内通过MDA-5信号通路来诱导机体产生S蛋白特异性的CD8+ T细胞13,这种免疫反应可能有助提高疫苗效力的持久性。重要的是,mRNA疫苗的成分除了需要精心设计,也需要一个灵敏而强大的平台来评估它们的免疫原性,以确定mRNA疫苗的初步安全性和有效性。InvivoGen提供了一系列的PRR报告细胞,可以帮助测试纳米材料和mRNA制剂的免疫刺激特性,例如我们的HEK293衍生的TLR3和TLR7报告基因细胞被Coolen et al.用来比较两种不同纳米颗粒材料的mRNA疫苗的免疫激活14;Son et al.采用了InvivoGen的HEK293衍生的TLR4和TLR7报告基因细胞系来检测不同mRNA纳米载体在TLR信号通路的参与15(产品信息请参见下文)。
References
1.U.S. Food and Drug Administration, 2022. Regulatory information, FDA-2020-D-1137. 2.Wolff, J.A. et al. 1990. Science 1990, 247, 1465–1468. 3.Rosa, S.S. et al. 2021. Vaccine, 39(16), 2190-2200. 4.Hou, X. et al. 2021. Nat Rev Mater 6, 1078–1094 (2021). 5.Vlatkovic, I. et al. 2021. Biomedicines, 9(5), 530. 6.Karikó, K. et al. 2008. Molecular therapy, 16(11), 1833-1840. 7.Andries, O. et al. 2015. Journal of Controlled Release, 217, 337-344. 8.Igyártó, B.Z. et al. 2021. Current opinion in virology, 48, 65-72.
地 址: 深圳福田区梅华路105号多丽工业区科技楼605 联系人: Miss Yao 电 话: 0755-26755892(深圳) 010-88594029(北京) 021-34613729(上海) 020-87615159 (广州) 传 真: 0755-26755877 Email:market@neobioscience.com
欣博盛生物科技有限公司
商家主页
