青春永驻是人类追求的终极梦想,而衰老却无处不在、不可阻挡、不可逆转。
人类对于长生的期盼自古就存在,秦始皇嬴政执着于对长生不老药的追寻,古埃及金字塔的修建也是另一种形式对长生的渴望。虽然目前我们还无法达到长生不老的水平,但也从未停止对延缓衰老的探索,随着科学的发展或许能让延缓衰老成为可能。世界各国研究者也致力于衰老生物学的研究,旨在发现衰老的驱动因素,筛选出一些潜在的“不老药”,从而达到延缓衰老、提高生命质量的目的。
作为一种半必需的微量氨基酸的牛磺酸(Taurine),它与衰老之间的关系在先前的研究中也显示出规律。有研究表明牛磺酸其代谢物在机体内的浓度会随着年龄的增长而下降,而外源补充牛磺酸对代谢和炎症性疾病有益[1,2],而机体牛磺酸缺乏,易引起骨骼肌、视网膜和中枢神经系统的功能障碍及衰老相关疾病的发生[3,4]。基于上述衰老过程中牛磺酸丰度的下降及其已知的健康影响的发现,来自印度国家免疫学研究所的Vijay K. Yadav团队近日在Science杂志上发表了一篇题为“Taurine deficiency as a driver of aging”的文章,通过不同物种中牛磺酸含量变化来探索牛磺酸缺乏是否是衰老的驱动因素并影响健康寿命[5]。

下面我们一起来看研究结果~
01牛磺酸缺乏是衰老的驱动因素
为了全面研究牛磺酸丰度是否影响健康寿命,研究人员测定了小鼠、猴子和人类不同年龄的血清牛磺酸浓度,发现血清牛磺酸浓度与年龄呈负相关(图1. A-C)。对14月龄小鼠补充牛磺酸,则可以延长这些小鼠的寿命(中位数10-12%,图1. D, E)。这种牛磺酸缺乏可能是衰老驱动因素的现象,不仅在哺乳动物中得到验证,在随后的线虫研究中也出现了相似的结果(图1. F)。这些结果表明,牛磺酸对寿命的影响在无脊椎动物和哺乳动物是相同的。
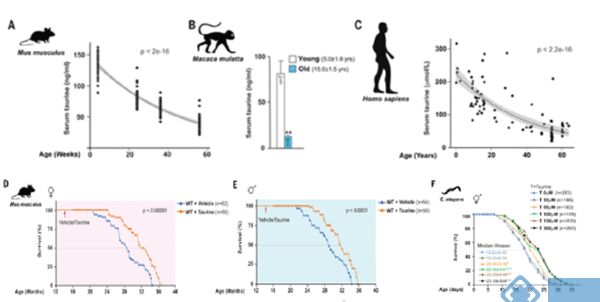
图1 牛磺酸缺乏是不同的物种衰老的驱动因素
02补充牛磺酸可以延长野生雌性小鼠健康寿命
与简单生存时长的延续相比,有意义的抗衰老疗法应该改善健康的生活时期。为了评估牛磺酸补充剂对健康生活时期的影响,研究人员对14月龄的小鼠进行持续10-12个月牛磺酸补充剂饲喂,随后通过功能测定及组织分析来分析骨骼,肌肉,大脑,胰腺,脂肪,肠道和免疫系统的健康状况。与对照组相比,牛磺酸补充组小鼠体重增加降低(图2. A, B)、骨量增加(图2. C)、肌肉力量增加(图2. E, F);悬尾实验、明暗箱实验和Y形迷宫实验结果显示,牛磺酸补充组小鼠抑郁样行为较少、探索好奇心更强(图2. G, H);葡萄糖耐量实验和胰岛素耐受性实验结果显示,牛磺酸补充组小鼠代谢葡萄糖能力及胰岛素敏感性都有明显改善(图2. I),且胃肠道转运速度更快(图2. J)。除此之外,补充高剂量牛磺酸对衰老个体中出现的炎症状态相关的髓系白细胞异常有改善作用(图2. K)。基于以上结果表明中年小鼠补充牛磺酸不仅可以改善多器官功能,还能延长其健康寿命。
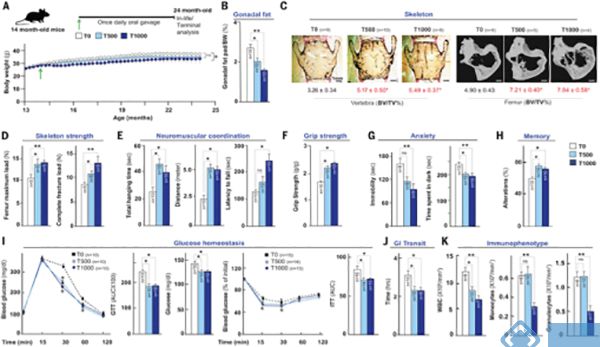
图2 补充牛磺酸可增加小鼠的健康寿命
03牛磺酸延长健康寿命的作用机制
基于上述发现,研究人员进一步对牛磺酸影响细胞功能以延长健康寿命的机制进行了探究。首先对野生型和牛磺酸缺陷小鼠中可以大量表达牛磺酸转运蛋白(由Slc6a6编码)的成骨细胞进行转录组测序(RNA Sequencing, RNA-seq)。牛磺酸缺陷小鼠成骨细胞RNA-seq分析显示,端粒功能,氧化应激,免疫功能,蛋白质翻译和干细胞维持等途径与野生型小鼠成骨细胞存在明显差异(图3. A)。除此之外,研究人员还构建了先天性牛磺酸缺乏小鼠模型(Slc6a6−/−)探究衰老细胞的积累是否诱导牛磺酸缺乏的小鼠健康寿命受损。与野生型小鼠相比,Slc6a6−/−小鼠寿命较短。对Slc6a6−/−小鼠进行清除衰老细胞的senolytic治疗,治疗后的小鼠寿命只增加了约21%,这一结果说明牛磺酸还影响衰老以外的其他因素(图3. B)。
为了进一步发现牛磺酸和其他衰老特征分子及细胞特征之间的关系。研究人员构建了端粒酶缺陷的斑马鱼模型(Tert-/-)来探究牛磺酸是否影响端粒酶缺乏引起的机体健康恶化,结果显示大约40%的鱼在受精后10天内死亡,而补充牛磺酸能显著提高存活率、抑制衰老进程(图3. C-E)。随后,基于小鼠模型的验证实验发现补充牛磺酸可以降低血清8-羟基脱氧鸟苷(8-hydroxydeoxyguanosine, 8-OH-dG)丰度,抑制DNA损伤(图3. F);可以提高DNA损伤后小鼠的存活率(图3. G);可以影响甲基化模式,改变染色质构象,进而影响衰老过程中的转录改变(图3. H);可以降低肝脏、棕色脂肪等组织中RS6P的磷酸化,维持蛋白稳态(图3. I);可以降低促炎因子水平,防止衰老过程中产生的促炎状态(图3. J);可以增加常驻干细胞的数量,进而提高某些组织的再生能力(图3. K);可以降低ROS诱导的脂质过氧化和蛋白羰基化,促进线粒体稳态(图3. L)。
基于已有的研究报道,胞质牛磺酸被转运到线粒体后,与tRNALeu的特定尿苷残基结合形成tm5U-tRNA,tm5U修饰对线粒体tRNAs具有独特性,并且它能促进电子传递链复合体I亚基ND6的翻译。研究人员测量了tm5U-tRNA修饰在小鼠衰老过程中是否发生变化,结果显示:与年轻小鼠肝脏相比,老年小鼠肝脏中tRNAs的tm5U含量下降超过60%以上,而补充牛磺酸的小鼠仅下降了20%左右(图3. M)。ND6蛋白翻译水平也显示出相同的趋势,随后的蠕虫实验也进一步提示牛磺酸可能通过增加线粒体复合体I的活性来促进健康(图3. N, O)。
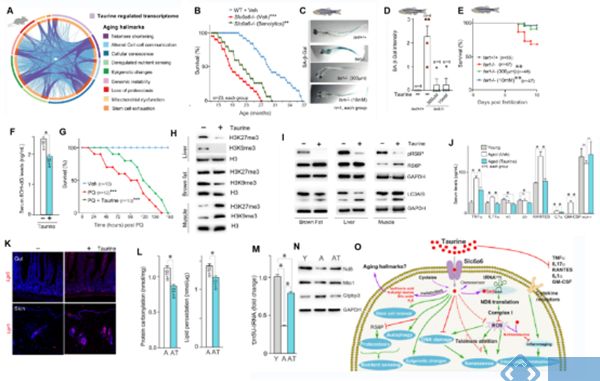
图3 牛磺酸对健康寿命的调节与多种衰老标志的改变有关
04牛磺酸在灵长类生物中的作用潜力
为了确定牛磺酸及其代谢产物(次牛磺酸和N-乙酰基牛磺酸)的血液水平是否与人类的健康变量相关,研究人员对11966名受试者的牛磺酸及其代谢物水平与50多个临床风险因素进行了关联分析,结果显示血液中牛磺酸及其相关代谢物水平较高的受试者,其体重指数(body mass index, BMI)较低、肥胖水平较低、2型糖尿病患病率较低、炎症水平较低(图4. A)。随后,作者通过对运动员和久坐人群的血清牛磺酸代谢物浓度的分析来探究牛磺酸水平是否会对运动产生响应,而运动是已知的可改善健康的干预措施。结果显示:无论是运动员组还是久坐不动组,运动后其血清中牛磺酸及次牛磺酸的浓度都出现增加(图4. B-D),这些结果表明牛磺酸和牛磺酸相关代谢物的增加可能介导运动带来的相关益处。最后,研究人员通过饲喂老年恒河猴来探究牛磺酸在非人灵长类动物中是否具有健康和抗衰老作用。通过持续6个月的牛磺酸补充,发现与对照组相比,补充牛磺酸组脂肪比例下降,骨密度增加,血糖浓度下降,肝损伤标志物浓度下降,随年龄增加的白细胞、单核细胞和粒细胞的数量出现下降,ROS诱导分子损伤的间接标志物8-OH-dG浓度下降,脂质过氧化物及蛋白质羰基浓度下降(图4. E-O)。

图4 牛磺酸途径影响灵长类动物的健康寿命
总的来说,以上结果表明牛磺酸浓度随着衰老进程而降低,而补充牛磺酸可以抑制这种下降,增加不同物种的健康寿命,这也确定了牛磺酸缺乏是这些物种衰老的驱动因素,而补充牛磺酸可以作为延缓衰老的一种潜在治疗策略,如果想要在临床中应用,仍需进一步进行随机对照的临床试验,以评估牛磺酸的抗衰老作用。
结语
作为组成生命物质基础蛋白组的基本组成单位,氨基酸在生命体的生长发育过程中起到至关重要的作用,各种类氨基酸与衰老之间的关系也被研究者关注。除了本研究表明的牛磺酸和衰老过程有显著的联系,先前有研究报道限制饮食中蛋氨酸及支链氨基酸(Branched chain amino acid, BCAA),可以改善胰岛素抵抗、氧化应激增加等多种衰老标志现象[6]。今年3月份厦门大学张杰、冷历歌团队通过研究发现补充D-丝氨酸,可以促进下丘脑中Menin蛋白的表达,有助于提高机体的代谢稳态,从而阻碍衰老进程的加速[7]。因此了解各类氨基酸在生物体中的浓度变化可以有效监测生物体的生理和病理状态。
